科学的な解析をするためには、まず化学物質の基礎的な性質について理解しておく必要があります。
例えば身近な物質として水や二酸化炭素などが代表的といえますが、これらに関するさまざまな知識を身に着けておくといいです。
中でもここでは「水や二酸化炭素には極性があるのか?無極性なのか?またその理由は?」について解説していきます。
水(H2O)が極性分子である理由【極性】
まず、水に極性があるかどうかを考えるためには、まずその化学構造を考えなければいけません。
そして、水の分子の形状は以下のような折れ線系の形をしているといえます。
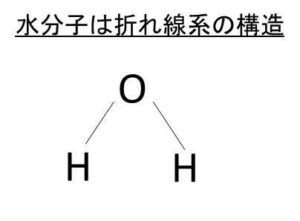
このとき、水分子の中心に来る酸素原子(O)の電子の数は6個であり水素との結合一つにつき、1個分の電子がくっついており、残り4個分の電子が余った状態となっています。すると、酸素原子はsp3混成軌道と呼ばれる状態(メタンの正四面体と同じようなもの)になり、かつ水素が二つ分であるため、残りの二つの軌道には何も入っていないような状況になるわけです。
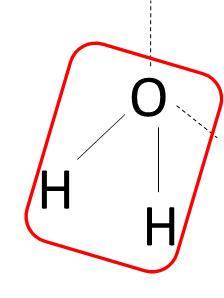
このように、水分子が折れ線になるわけですが、さらにOH結合ではO(酸素)の方が電気陰性度が高く電子をより引き付けているといえます。このとき、上述のように水分子は折れ曲がった構造をしているため、水の分子全体としてみたとしても、極性が残ったままになるといえます。
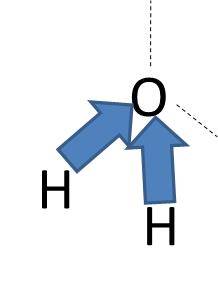
このような理由から、水分子には極性がある極性分子であると説明できるのです。
どのような物質でも、分子の構造と結合間の極性(電気陰性度の差)を考えると、極性分子なのか無極性分子なのかという理由がわかることを覚えておきましょう。
二酸化炭素(CO2)には極性が無い理由【無極性分子】
続いて、二酸化炭素(CO2)が無極性分子である理由についても確認していきます。
先ほどと同様にまずは二酸化炭素の分子の形自体を考えます。すると、以下のような直線形状の構造をしていることがわかるでしょう。
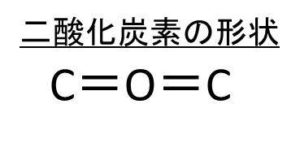
続いて、CO間の電気陰性度の差を考えていきます。こちらも酸素原子Oの方が電気陰性度の大きさが高いためにこちらに電子が引き寄せられることになるのです。
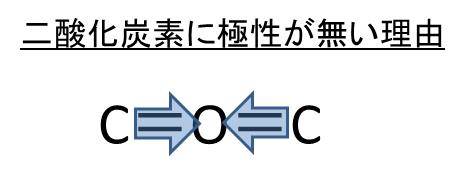
ただ、二酸化炭素の構造は見ての通り、対象な形をしているために結局のところ、C=O間の結合が分子全体では相殺されることになってしまうわけです。
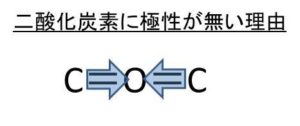 つまり、二酸化炭素は極性が無い無極性分子であることがわかりました。
つまり、二酸化炭素は極性が無い無極性分子であることがわかりました。
まとめ
ここでは、水が極性分子である理由と、二酸化炭素には極性が無い理由(無極性分子)について確認しました。
水に極性があるのはその化学構造が折れ線であり、かつOH結合に電気陰性度の差(極性)があるためといえます。
一方で、二酸化炭素は分子の形が直線であり、対象であるために無極性分子となるのです。
身近な物質の物性を理解して、より科学を楽しめるようになっていきましょう。

コメント